繳費方式
現金/支票:請至系統下載審查費繳款單,填妥後上傳系統→秘書行政審查時IRB檢核並蓋章(系統)→至誠愛樓14F財管室出納組繳費→將收據影本上傳至系統。
註1:支票抬頭為「中山醫學大學附設醫院」
註2:IRB不再協助繳費,委託快遞協助繳費者,請確認繳款單是否已核章。
轉帳(匯款):轉帳(匯款)完成→至「IRB審查費轉帳(匯款)開立收據資訊登錄」填寫匯款資訊以供對帳→秘書協助上傳收據並通知收據正本取回。
Ø 帳號資訊:彰化銀行北台中分行(銀行代碼009,帳號:4004-86-088960-00,戶名:中山醫學大學附設醫院)。
Ø 開立收據相關流程須至少7個工作天,如為急件請以現金/支票自行繳費辦理。
Ø 院校內收據請於收到收據開立完成通知7天內前來IRB簽收領取,廠商收據請自行派快遞取回,以免延誤收據核銷時間。
※依據院內財管室規範,收據如非開立錯誤,不得重新開立,院校內請留意三個月內核銷期限。
注意事項
- 請於案件審查完畢前完成繳費,除中山附醫醫研部及國科會獎補助計畫。
※ 中山附醫醫研部:採院內扣款,不需繳費,請編列足夠審查費。
※ 國科會計畫待獎補助通過後再繳,未通過者免繳。
Ø 未通過要繼續執行:變更經費來源並繳交審查費(主持人自行發起)。
Ø 未通過不要執行:申請終止。 - 進入審查流程的案件需完成繳費,審查中若主持人欲撤回申請案,恕不退費。
- 若未具體揭露經費來源、利益衝突或其它因素,而造成繳費金額認定錯誤,需補繳足額審查費用。
- 合約相關問題請洽臨床試驗中心,聯絡專線 04-36111407。
- 跨院校(多中心)合作之學術研究計畫(非產品),外院校或本院校之總主持人(Investigator Chair or Protocal Chair)亦兼具委託者與主持人(Sponsor-Investigator)兩種身分,責任重大,須監督管理各執行場所,整合分析各中心資料,請籌措足額研究經費資源再執行,以維護研究執行品質及研究對象權益。使用特定產品介入之學術研究多中心合作案,比照廠商委託案收費。
審查費用
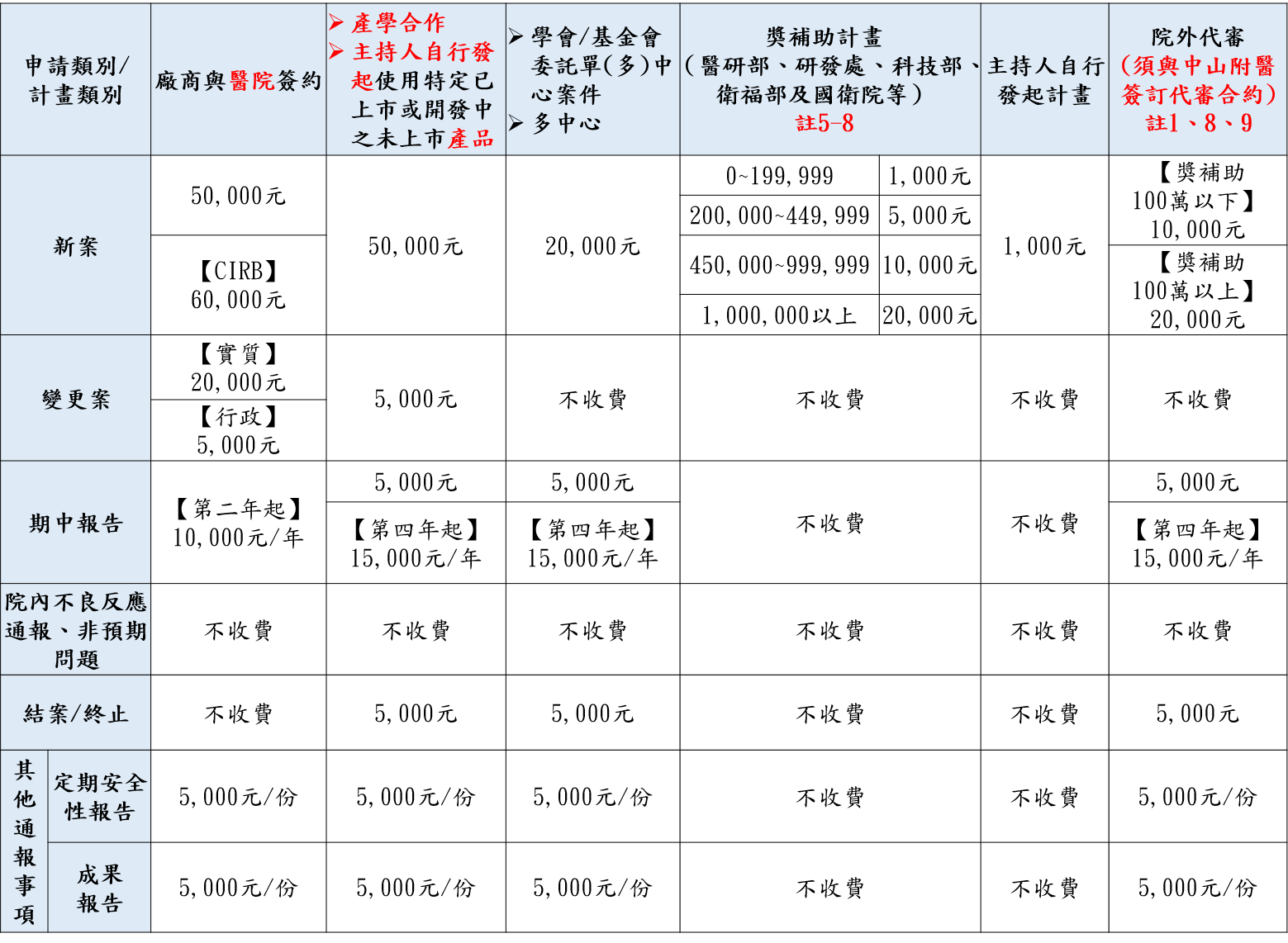
IRB收費標準(經以下會議決議:一O七年度八月份委員會議通過;一O七年度第三次臨床管理小組會議(107.10.15)通過修訂;一O七年度十月份高階主管會議通過;一O七年度第三次董事會議(107.12.06)通過修訂)
- 院外代審案件涉及產品比照廠商案收費標準。
- 廠商因故延遲結案,逾越原IRB許可函效期,請編列經費,比照試驗延長案收費辦理。
- CIRB或廠商贊助案件多版變更案合併送審,針對 (1)主持人手冊 (2)計畫書 (3)個案報告表之文件,採逐案收費。
- CIRB案件自IRB發出審查意見之隔日起計算,務必於二個工作日內完成回覆,逾期回覆,需額外繳交延遲作業費用(一日5,000元整,二日合計10,000元整,三日合計20,000元整,超過三日委員會得不再受理)。敬請試驗委託者於送審前,審慎評估;否則,得以一般程序送審。(NRPB與中區聯盟案件,選擇本院為主審醫院,回覆時間不受此限)
- 醫研部獎補助計畫直接由財管室統一扣款。
- 獲得單位獎補助之主持人,應檢附核定金額證明,由IRB開具通知,至財管室辦理繳款。
- 未獲得獎補助者,得向IRB辦理終止,免收審查費。若要繼續執行,請提變更案變更經費來源為主持人自行發起,收費標準比照主持人自行發起計畫辦理。
- 政府(其它)獎補助對象非本醫院學校,該獎補助經費亦未進入本醫院或學校財務單位進行核銷者,視同校院外合作案辦理,請參照院外代審收費辦法。
- 「代審」係指簽立委託中山附醫IRB代審合約之外院校機構,委託本醫院IRB代理審查及管理該院校機構之人體研究(試驗)。
- 本院校內主持人離職,案件尚未結束,比照外院校主持人收費。
- 申請委員名單、調閱、複印特定資料及許可書勘誤等,每份收費5000元。
- 安全性通報不屬於變更案,請以「安全性通報」送審。本院受試者發生之SUSAR、non-SUSAR通報不收費;但非本機構SAE︰包括國外或國內它院SUSAR/SAE(個案)、Periodic SUSAR / SAE report (PSUR)、 Clinical Trial Line Listing、DSMB report、及安全性相關文件等,非屬本國法規規範之必要送審文件,請廠商評估送IRB之必要性,若自主決定送IRB審查,需繳交審查及行政作業費每份5000元。
- 結案後文件每份收費5000元。
- IRB始受理送審文件,若撤回申請案,或繳交文件不齊全致無法完成審核時,均不退費,請審慎考慮。
註:
- IIT(investigator-initiated trial)是學術機構裡的醫師研究者自行發掘問題、設計、執行、資料分析、判讀、發表。比較偏向獨立的研究。
- IIS(Investigator initiated study; IIS))本國(或多國)多中心試驗是由多位研究者(計畫主持人及總主持人)按同一計畫書,於不同地點及單位執行臨床試驗;研究者自發行研究(Investigator initiated study; IIS) 之總主持人負全責,本機構主持人針對本院研究對象(受試者)負責。IIS不適用於查登案。
- 產學合作:廠商與學校簽約
